
Element ve bileşikler saf maddelerdir.
SAF MADDE:Aynı cins atom veya moleküllerin bir araya gelmesi ile oluşan maddelere saf maddeler denir.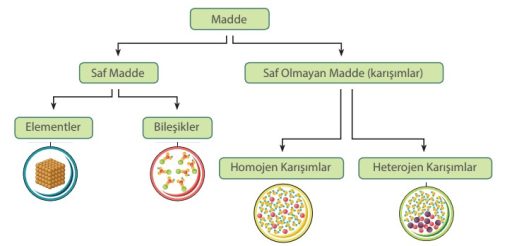
- Tek cins atomlardan oluşan maddelerdir ve elementi oluşturan atomların bütün özellikleri aynıdır.

- Elementler fiziksel ve kimyasal yollarla ayrılamazlar.
- Semboller ile gösterilir ve bu semboller tüm Dünyada ortak gösterime sahiptir. Dillere göre sembol farklı elementi ifade etmez.
- farklı elementlerin atomları farklı özelliktedir. Örneğin altın elementi atomları ile bakır atomları farklı özelliktedir.
- Aynı elementlerin atomlarından oluşan moleküllere element molekülü denilir.
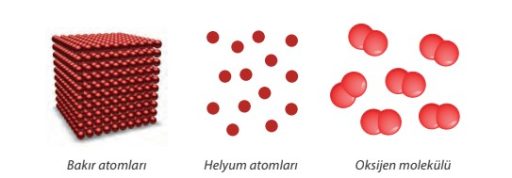
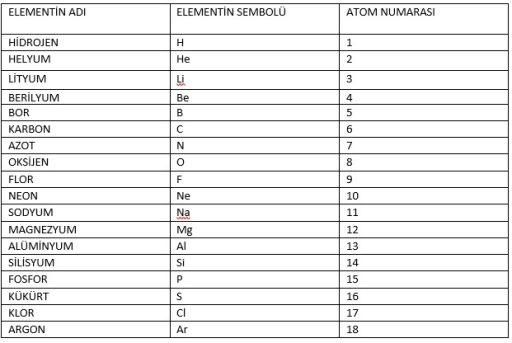
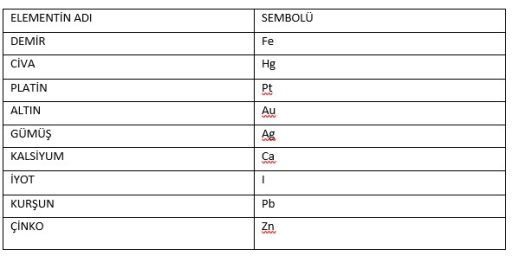
Atom numarası atomun kimliğini belirler.
BİLESİKLER
Bileşikler
- Farklı CİNS atomların kimyasal yollarla bir araya gelerek oluşturdukları yeni maddelere bileşik denir.
- Bileşikler kendilerini oluşturan elementlerin özelliklerini taşımazlar. Yepyeni bir madde olurlar.
- Saf ve homojen maddelerdir.
- Formüllerle gösterilirler.
- kimyasal yollarla ayırılabilirler .
- Bileşiği oluşturan elementler belli bir oranda bir araya gelirler.
- Bileşikler saf madde oldukları için belli bir erime, kaynama ve donma noktaları vardır.
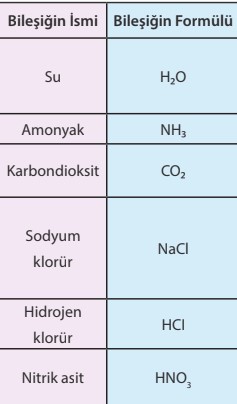
SU: Su molekülünde 2 farklı element, toplam 3 atom vardır. (H VE O)
NİTRİK ASİT:3 Farklı element(H,N VE O) toplam 5 atom vardır.
SAF OLMAYAN MADDELER(KARIŞIMLAR):
- Birden fazla FARKLI CİNS atomların bir araya gelerek kimyasal bağ kurmadan oluşturdukları topluluktur.
- Bir araya gelen maddeler özelliklerini kaybetmezler.
- Formülleri veya sembolleri yoktur.
- Fiziksel yollarla bileşenlerine ayrışırlar.
- HOMOJEN(ÇÖZELTİ) VE HETEROJEN olmak üzere iki karışma şekline sahiptir.
HOMOJEN KARIŞIM: Bir araya gelen maddeler eşit şekilde dağılıyorsa (biri diğerinin içinde çözünüyorsa) oluşan karışım homojendir.
ÖRNEK: Şekerli su, tuzlu su ,alkol su karışımı, gazoz homojen karışımlardır.

Homojen karışımlar aslında birer çözelti örneğidir.
ÇÖZELTİ:Bir maddenin diğer madde içinde dağılmasıdır.
ÇÖZÜNME HIZINI ETKİLEYEN FAKTÖRLER:
1-TEMAS YÜZEYİ: Temas yüzeyi arttıkça çözünme hızı artar.
2-SICAKLIK: Sıcaklık arttıkça çözünme hızı artar.
3-KARIŞTIRMAK:Çözeltiyi karıştırmak çözünme hızını arttırır.
HETEROJEN KARIŞIM: Karışımı oluşturan maddeler her yere eşit dağılmıyor ise oluşan karışım heterojen karışımdır.
ÖRNEK: Zeytin yağı-su ,ayran, süt, Türk kahvesi, çorba

NOT: Karışımlar fiziksel yöntemlerle bileşenlerine ayrılır.
1-BUHARLAŞTIRMA YÖNTEMİ: Katı-sıvı homojen karışımları(tuzlu su, şekerli su gibi)ayırmak için kullanılan en iyi yöntemdir. Çözeltiyi ısıtırsak sıvı buharlaşır ve dipte katı madde kalır bu sayede katı sıvıdan ayrışır.

2-YOĞUNLUK FARKI İLE AYIRMA: Birbiri içinde çözünmeyen sıvı-sıvı heterojen karışımlar yoğunluk farkından yaralanarak ayırılır. Yoğunluğu fazla olan sıvı kabın altında, az olan sıvı kabın üstünde kalır ve ayırma hunusine koyarak ayırma gerçekleşir.

Görselde su ve zeytinyağı verilmiştir. Yoğunluğu fazla olan su altta, az olan zeytinyağı üstte durmaktadır. Huninin musluğu açılır su alttaki kaba akar ve musluk kapatılır bu sayede sıvılar ayrılır.
DAMITMA YÖNTEMİ İLE AYTRMA: Bu yöntemde birbiri içinde çözünen sıvı-sıvı homojen karışımları KAYNAMA NOKTALARI FARKNDAN yararlanarak ayırırız.

Görselde 1 numaralı kapta ALKOL -SU karışımı vardır kaynama noktası düşük olan alkol daha çok buharlaşır ve 2 numaralı kapta toplanır. Bu işlem tamamen ayırabilmek için birkaç kere tekrarlanabilir. Sonuç olarak kaynama noktası küçük olan sıvı 2. kapta toplanır.
Bir Cevap Yazın